引言
表观吸收效率(AEA)长期以来被用作评估新生犊牛初乳IgG转移成功与否的一种实用指标。其计算方法很简单:估算犊牛在采食后体内“表观存在”的IgG量,用其除以摄入的IgG量,并以百分比表示。这个指标非常有用,因为它可以帮助我们比较不同犊牛、不同饲喂方案,并评估管理水平。然而,“表观”这个词非常重要。
首先,我们来看一些背景。我们通常利用AEA来预测犊牛在出生后某一时间点的血清IgG浓度:
IgG摄入量等于初乳中IgG浓度乘以摄入的初乳量,而血浆体积通常根据体重(kg)乘以一个系数来估算,常用值为9%
IgG摄入量等于初乳中IgG浓度乘以摄入的初乳量,而血浆体积通常根据体重(kg)乘以一个系数来估算,常用值为9%。
我们也可以将公式重排来计算AEA:
表观吸收效率(%) =(血清IgG(g/L)× 血浆体积(L))/ IgG摄入量(g)× 100
AEA用于估计犊牛从初乳中吸收IgG的效率。有些犊牛每单位摄入IgG能吸收更多,而有些则较少。因此,这是评估牧场初乳管理的重要指标。诸如产前热应激(Tao等,2012;Dado-Senn等,2020)、初乳巴氏消毒(Elizondo-Salazar和Heinrichs,2009;Robbers等,2021)、难产(Waldner等,2009;Murray等,2015)等因素,均已被报道会影响AEA。
然而,AEA并不是IgG通过肠壁的直接测量值。它是基于血清或血浆中IgG浓度,并结合血浆体积估算得出的结果。这意味着,该数值不仅受肠道吸收影响,还受IgG在体内液体中分布方式的影响。因此,AEA不仅仅是肠道吸收的指标,它同样反映了IgG在犊牛体内的分布情况。这一点有助于解释为什么AEA不会达到100%,为什么不同犊牛之间差异较大,以及其中一部分变异可能来源于吸收之外的生理过程。
基本概念
当犊牛摄入初乳后,免疫球蛋白G(IgG)通过胞饮作用从肠道进入体内。然而,一旦被吸收,IgG并不会仅停留在血液中,而是会分布在至少两个主要的液体区室中:
- 血管内空间(即血浆)
- 血管外空间(包括血管外的组织间液)
当我们在某一时间点测量血清IgG时,实际上只是在测量该时刻血管内空间中的IgG浓度。我们并不是在测量体内总吸收的IgG量,而是在测量某一特定时间点血管内空间中存在的IgG量。
这非常重要,因为血清浓度取决于两个因素:
- 吸收的IgG总量
- IgG分布到的液体体积
因此,两头犊牛可能吸收了相似数量的IgG,但如果IgG在血管内和血管外空间中的分布不同,其血清IgG浓度可能不同。
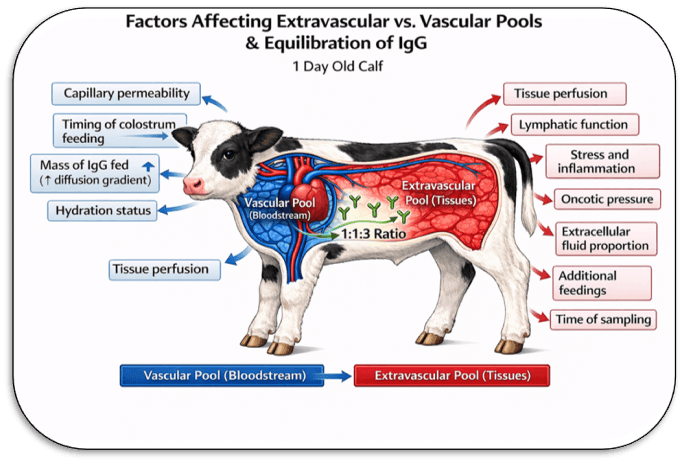
“血管外空间”
从生理学角度来看,体液通常分为细胞内液和细胞外液。细胞外液包括血浆(血管内)和组织间液(血管外),而细胞内液则存在于细胞内部。这些区室通常通过特定标记物进行估算。
研究表明,犊牛体内总水分约占体重的72%至88%(Thornton和English,1975)。其中,大部分水分位于细胞外液中——有研究指出,80%以上的总水分属于细胞外液(Wagstaff等,1992)。然而,在这些液体中,只有一小部分位于血管内空间,也就是我们测量血清IgG的地方。
在评估IgG吸收时,我们通常使用血浆体积(PV),它属于细胞外液的一部分。血浆体积通常通过Evans Blue染料(Thornton和English,1978;Wagstaff等,1992;Quigley等,1998;Cabral等,2015)或¹³¹I标记白蛋白(Möllerberg等,1975)来测量。
为了更好地理解IgG吸收,我们可以将系统简化为两个功能性区室:血管内空间(测量IgG的地方)和血管外空间(IgG可能分布的地方)。
以一头1日龄、体重40 kg的犊牛为例:
- 体重 = 40 kg
- 总水分 = 40 × 0.75 = 30 kg
- 细胞外液 = 30 × 0.80 = 24 kg
- 细胞内液 = 6 kg
- 血浆体积 = 40 × 0.09 = 3.6 kg
- 组织间液 = 24 − 3.6 = 20.4 kg
因此,该犊牛约有24 kg细胞外液,但只有3.6 kg位于血管内。组织间液与血浆的比例约为5.7:1,即血管外液体体积约为血浆的6倍。
分布容积(Vd)
在药理学中,物质在血管内与血管外之间的分布通常用“分布容积(Vd)”来描述。该值表示物质从血液进入组织和体液的程度。需要注意的是,Vd并不一定代表真实的解剖体积,而是表示在测量时物质“表观分布”的体积。
这一概念同样适用于新生犊牛的IgG。虽然血管外液体空间远大于血浆体积,但IgG并不会立即或完全分布到整个空间中。实际观察到的分布比例约为1.3:1,远低于解剖学比例,这说明在测量时IgG仅与部分血管外空间达到了平衡。
IgG确实会分布到血管外液体中(包括组织间液),这一点已在多个物种中通过淋巴和组织液测量得到证实。因此,血清IgG浓度反映的是吸收与分布之间的平衡,而不仅仅是吸收。
为什么AEA不会达到100%
在实际条件下,甚至在理想实验条件下,AEA也不应达到100%。原因包括:
首先,并非所有摄入的IgG都能被吸收。肠道吸收本身就是不完全的过程。
其次,AEA基于血浆中的IgG,而非体内总IgG。如果IgG在采血时已部分分布到血管外空间,则血浆测量会低估总吸收量。
第三,IgG的分布是动态的。随着IgG在血管内外之间移动,血清浓度会随时间变化,即使体内总量不变。
一个动态系统,而非静态
IgG吸收并不是一个简单事件,而是一个动态过程。
血清IgG浓度只是这一动态系统在某一时间点的“快照”。
总结
AEA和血清IgG都是对一个动态系统的估计。它们不仅反映IgG的吸收,还反映其在体内的分布。
参考文献
Cabral, R. G., C. E. Chapman, E. J. Kent, and P. S. Erickson. 2015. Estimating plasma volume in neonatal Holstein calves fed one or two feedings of a lacteal-based colostrum replacer using Evans blue dye and hematocrit values at various time points. Can. J. Anim. Sci. 95:293-298 doi:10.4141/CJAS-2014-176 293.
Dado-Senn, B., L. Vega Acosta, M. Torres Rivera, S. L. Field, M. G. Marrero, B. D. Davidson, S. Tao, T. F. Fabris, G. Ortiz-Colón, G. E. Dahl, and J. Laporta. Pre- and postnatal heat stress abatement affects dairy calf thermoregulation and performance. J. Dairy Sci. 103:4822-4837. https://doi.org/10.3168/jds.2019-17926.
Elizondo-Salazar, J. A., and A. J. Heinrichs. 2009. Feeding heat-treated colostrum or unheated colostrum with two different bacterial concentrations to neonatal dairy calves. J. Dairy Sci. 92 :4565–4571 doi:10.3168/jds.2009-2188.
Möllerberg, L., L. Ekman and S. Jacobsson. 1975. Plasma and blood volume in the calf from birth till 90 days of age. Acta Vet. Scand. 16:178-185.
Murray, C. F., D. M. Veira, A. L. Nadalin, D. M. Haines, M. L. Jackson, D. L. Pearl, and K. E Leslie. 2015. The effect of dystocia on physiological and behavioral characteristics related to vitality and passive transfer of immunoglobulins in newborn Holstein calves. Can. J. Vet. Res. 79:109–119.
Quigley, J. D. III, J. J. Drewry, and K. R. Martin. 1998. Estimation of plasma volume in Holstein and Jersey calves. J. Dairy Sci. 81:1308-1312.
Robbers, L., R. Jorritsma, M. Nielen, and A. Koets. 2021. A scoping review of on-farm colostrum management practices for optimal transfer of immunity in dairy calves. Front. Vet. Sci., 18 July 2021. 8-2021. https://doi.org/10.3389/fvets.2021.668639.
Tao, S., A. P. A. Monteiro, I. M. Thompson, M. J. Hayen, and G. E. Dahl. 2012. Effect of late-gestation maternal heat stress on growth and immune function of dairy calves. J. Dairy Sci. 95:7128–7136. http://dx.doi.org/ 10.3168/jds.2012-5697.
Thornton, J. R., and P. B. English. 1978. Body water of calves: Change in distribution with diarrhoea. Br. Vet. J. 134:445-453.
Wagstaff, A. J., I. Maclean, A. R. Michell, and P. H. Holmes. 1992. Plasma and extracellular volume in calves: comparison between isotopic and ‘cold’ techniques. Res. Vet. Sci., 53:271-273.
Waldner, C. L., and L. B. Rosengren . 2009. Factors associated with serum immunoglobulin levels in beef calves from Alberta and Saskatchewan and association between passive transfer and health outcomes. Can Vet J. 50:275–281.