Clique aqui para obter uma versão em PDF
Autor: Jim Quigley
Traduzido por: Ana Luiza Resende e Rafael Azevedo
Introdução
As vitaminas lipossolúveis são essenciais para os bezerros jovens e devem ser incluídas tanto nos substitutos do leite quanto nas rações iniciais. As principais vitaminas lipossolúveis – A, D e E – são essenciais para a saúde e o crescimento dos bezerros e devem ser incluídas nos substitutos do leite, nas rações iniciais e nas rações de crescimento.
Realizei uma revisão da literatura científica sobre as vitaminas A, D e E e analisei as recomendações do comitê do NASEM de 2021 no documento “Nutrient Requirements for Dairy Cattle” (Requisitos de nutrientes para gado leiteiro) (NASEM, 2021). Para avaliar as recomendações do NASEM, utilizei vários modelos de crescimento de bezerros e determinei as necessidades com base na ingestão de ração líquida e seca em várias idades, usando programas de alimentação típicos. Avaliei as necessidades mínimas de cada vitamina com base na ingestão tanto do substituto do leite quanto da ração inicial para bezerros para sempre atender ou exceder a recomendação do NASEM. Para obter mais informações sobre essa abordagem, consulte o Apêndice B na Calf Note #243. Aqui está um resumo da literatura e minhas recomendações (“Ajustadas”) quando elas diferem das do NASEM.
Vitamina E. O Comitê do NASEM recomendou uma concentração de vitamina E de 2 UI/kg de peso vivo, ou aproximadamente 125 UI/d (Tabela 1). Eles também afirmaram que essa taxa de suplementação pode ser inadequada para bezerros de crescimento rápido. Foi demonstrado que a taxa de ganho de peso corporal afeta a necessidade de vitamina E (NASEM, 2021). Assim, quando programas de alto crescimento são implementados (ou seja, programas que permitem um GMD >700 g), deve ser incluído um equivalente adicional de vitamina E.
As exigências recomendadas de vitamina E nas dietas de bezerros aumentaram à medida que os pesquisadores relataram o importante papel da vitamina na resposta imune dos bezerros (por exemplo, Reddy et al., 1987a,b). A vitamina E tem sido estudada com mais detalhes do que outras vitaminas desde a publicação do NRC de 2001. Grande parte do trabalho documentou uma função do α-tocoferol na promoção da resposta imunológica, principalmente fornecendo capacidade antioxidante ao animal e reduzindo os efeitos do estresse oxidativo na competência imunológica (Abuelo et al., 2019). Os efeitos da vitamina E suplementar sobre os índices da resposta imunológica (números de linfócitos, ativação de linfócitos, título de anticorpos em resposta à vacinação) foram relatados em bezerros Holandês e bezerros Wagyu japoneses (Otomaru et al., 2013; 2015). A vitamina E pode desempenhar um papel na maturação do sistema imunológico, conforme indicado pela produção de óxido nítrico por leucócitos mononucleares do sangue (Rajaraman et al., 1998). A produção de óxido nítrico em leucócitos juvenis é maior do que a de células maduras; a vitamina E pode desempenhar um papel na maturação dessas células para melhorar o possível dano celular causado pelo excesso de produção de NO. Por outro lado, Schmidt et al. (1998) não relataram nenhum efeito da suplementação de vitamina E (188 vs. 354 UI/d) na hematologia de bezerros vacinados com toxina Shiga com cinco e oito semanas de idade. Entretanto, Waldner et al. (2017) relataram que os bezerros com vitamina E sérica abaixo do adequado para a idade (2-7 dias de idade, <0,8 μg/mL; >7 dias de idade, <0,5 μg/mL) tinham 3,2 vezes mais probabilidade de serem tratados por enterite do que os bezerros com concentrações mais altas.
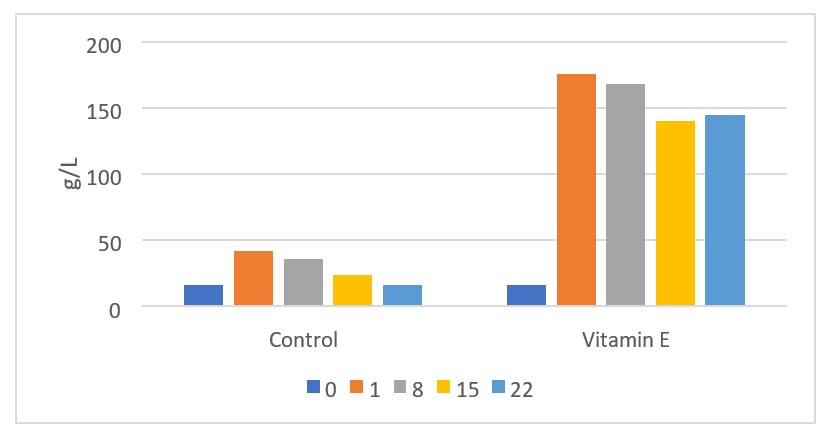
O status de vitamina E dos bezerros neonatos depende, em grande parte, da dieta de vacas secas e do consumo de colostro, que é a principal via de fornecimento de vitaminas lipossolúveis aos bezerros recém-nascidos (Quigley e Bernard, 1995). A suplementação de colostro aumentou o status de vitamina E dos bezerros recém-nascidos (Quigley e Bernard, 1995). Está claro que a variabilidade no conteúdo de gordura em geral e no conteúdo de vitaminas solúveis em gordura no colostro pode afetar a vitamina E e o status antioxidante dos recém-nascidos. Mohri et al. (2005) relataram que a injeção de vitamina E (300 U de acetato de α-tocoferol/45 kg de peso vivo) e selênio (6 mg/45 kg de peso vivo) alterou a hematologia de bezerros jovens, melhorando, em geral, o número de linfócitos e os índices de capacidade antioxidante. A vacinação de bezerros recém-nascidos da raça Jersey com 2.000 UI de vitamina E uma vez por semana durante as duas primeiras semanas de vida melhorou muito as concentrações de IgG no soro (Figura 1; Pekmezci e Cakiroglu, 2009). Concentrações séricas de IgG superiores a 100 g/L no início da vida sugerem um aumento dramático no início da imunidade ativa e devem ser consideradas supra fisiológicas.
Reddy et al. (1987b) recomendaram 125 UI/d como o nível ideal de suplementação para bezerros da raça Holandês. No entanto, as taxas de alimentação líquida nesse estudo foram baixas (ou seja, 8% do PV; Reddy et al., 1987a) e foi demonstrado que a necessidade de vitamina E aumenta com o crescimento (Nonnecke et al., 2010). Portanto, a suplementação com vitamina E ou equivalentes de vitamina E pode variar dependendo da taxa de alimentação do CMR e da taxa de crescimento projetada.
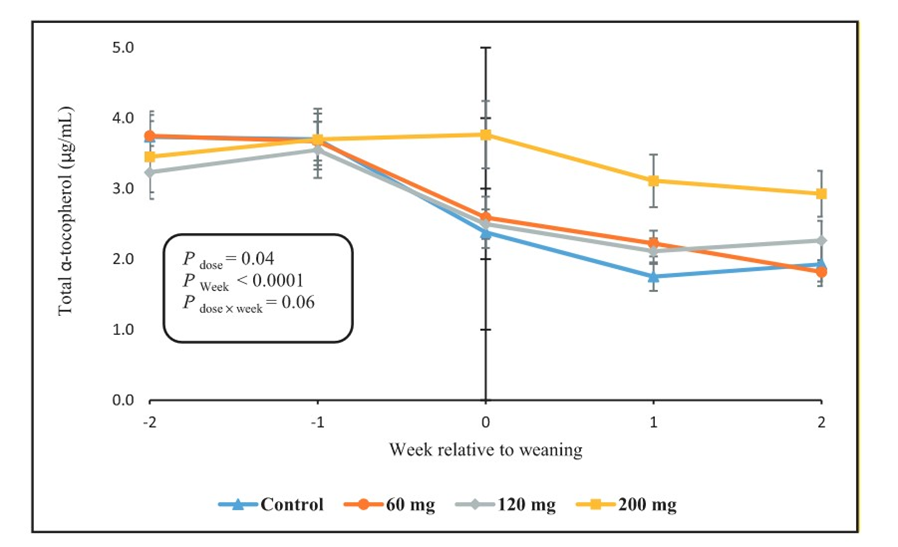
O desmame é uma transição importante na vida dos bezerros e o status antioxidante reduzido dos bezerros desmamados (Majlesi et al., 2021) pode ter efeitos deletérios na resistência a doenças após o desmame. Recentemente, Lashkari et al. (2022) relataram que a RRR-α-tocoferol plasmática era de 0,8 µg/ml no desmame (61 dias de idade). Em geral, as concentrações plasmáticas de vitamina E inferiores a 0,5 a 1,0 µg/ml são consideradas inadequadas na maioria das espécies (McDowell et al., 1996) e a vitamina E plasmática de 0,6 a 1,6 µg/ml pode resultar em distrofia muscular em bezerros (Adams, 1982). O declínio na vitamina E plasmática no desmame pode estar relacionado à transição de uma dieta rica em gordura (do leite ou substituto do leite) para uma dieta tipicamente contendo <5% de gordura em uma base de MS. Além disso, a natureza da gordura (potencialmente insaturada) pode interferir na absorção do α-tocoferol, fornecendo substrato inadequado para a micelarização durante a digestão e o transporte intestinal. Foi relatada má absorção de α-tocoferol após o desmame (Reddy et al., 1987a). A alimentação com 60 ou 120 mg/kg de RRR-α-tocoferol foi insuficiente para manter as concentrações plasmáticas de vitamina E, enquanto 200 mg/kg mantiveram os níveis plasmáticos por 2 semanas após o desmame (Lashkari et al., 2022; Figura 2). Esses autores recomendaram que as concentrações de α-tocoferol nas dietas fornecidas aos bezerros por volta do desmame deveriam ser de 200 mg/kg de MS. Esses autores também compararam fontes de vitamina E – 200 mg/d de RRR-α-tocoferol (ALC), 200 mg/d de acetato de RRR-α-tocoferil (ACT) ou 200 mg/d de acetato de all-rac-α-tocoferil (SYN). As concentrações de α-tocoferol plasmático no desmame foram de 2,7, 2,1, 1,1 e 0,8 µg/ml para ALC, ACT, SYN e Controle, respectivamente (Lashkari et al., 2022). Os autores concluíram que 200 mg/kg de ALC foi a inclusão mais eficaz para manter os níveis plasmáticos de vitamina E por volta do desmame.
Vitamina A. A nova recomendação do NASEM para a ingestão de vitamina A é de 110 UI por kg de peso vivo (Tabela 1) ou 11.000 UI/kg no substituto do leite e 3.700 UI/kg na ração inicial e de crescimento para bezerros (Tabela 2).
Kume e Toharmat (2001) relataram resultados com 46 bezerros Holandês no nascimento e aos 6 dias de idade. As concentrações de β-caroteno e vitamina A plasmática aumentaram do nascimento aos 6 dias de idade. O β-caroteno e a vitamina A plasmática foram positivamente correlacionados com a MS fecal, mas não foram observadas correlações entre as vitaminas plasmáticas e os componentes da eritropoiese. Esses resultados sugerem que o status de β-caroteno dos bezerros aos 6 dias de idade depende das concentrações de β-caroteno no colostro e afeta a ocorrência de diarreia, e o status de vitamina A depende da vitamina A colostral e da transferência de vitamina A da placenta durante a gestação. Eicher et al. (1994) relataram que a combinação de vitaminas A e E pode melhorar a função dos leucócitos de bezerros até 6 semanas de idade. Em termos de fabricação, a emulsificação das vitaminas lipossolúveis em geral, e da vitamina A em particular, melhora a absorção (Jacobson et al., 1954). Waldner et al. (2017) relataram que os bezerros com vitamina A sérica inferior a 0,14 μg/mL tinham 2,8 vezes mais probabilidade de morrer, indicando o papel que a vitamina A desempenha na resposta imunológica geral.
Vitamina D. A nova recomendação do NASEM para a ingestão de vitamina D é de 32 UI por kg de peso vivo (Tabela 1) ou 3.200 UI/kg em substitutos do leite e 1.100 UI/kg em bezerros na fase inicial e em crescimento (Tabela 2).
O status de vitamina D dos animais é indicado de forma confiável pela concentração do metabólito 25 hidroxivitamina D (25(OH)D) no soro ou no plasma, com uma concentração de 30 ng/mL proposta como um limite inferior para a suficiência. Os bezerros geralmente nascem com insuficiência de vitamina D (< 8 ng/ml de 25(OH)D) e podem permanecer nesse estado por até 3 meses (Flores-Villalva et a. 1021). Conforme resumido por Nelson et al. (2016), as concentrações de 25(OH)D no soro são de aproximadamente 15 ng/mL no nascimento e permanecem ≤15 ng/mL até um mês de idade se alimentadas com leite de descarte pasteurizado com pouca ou nenhuma exposição ao sol no verão. Em contraste, a 25(OH)D sérica de bezerros alimentados com substituto do leite contendo 6.600 e 11.000 UI de vitamina D3/Kg de matéria seca foi de
59 ± 8 e 98 ± 33 ng/mL, respectivamente, com 1 mês de idade (Nelson et al., 2019). Bezerros suplementados de forma semelhante indicaram que a 25(OH)D sérica alcançada com aproximadamente 1 mês de idade aumentaria de 6 a 7 ng/mL para cada 1.000 UI de vitamina D3/kg de matéria seca de substituto do leite. Blakely et al. (2019) sugeriram que a suplementação de leite de descarte pasteurizado com vitaminas A, D e E (0,25 ou 0,50 ml/dia de um produto contendo 50.000 UI de vitamina A como retinil-palmitato, 50.000 UI de vitamina D3 e 500 UI de vitamina E como RRR-α-tocoferol por mililitro de produto) mais 0,5 ml do mesmo suplemento injetado ao nascimento resultou em taxas de crescimento mais baixas aos 28 dias de idade do que os bezerros não suplementados, provavelmente devido ao excesso de suplementação vitamínica. Portanto, parece haver um limite superior para a suplementação com vitaminas lipossolúveis. Por fim, pesquisadores na China sugeriram que a alimentação com 25(OH)D no CMR aumentou o consumo de ração seca e crescimento mais rápido do que os controles não suplementados (mas de forma semelhante aos bezerros alimentados com vitamina D3) e reduziu os índices de estresse associados ao desmame aos 60 dias em comparação com os controles não suplementados (Xu et al., 2021; Wang et al., 2022).
Resumo e recomendações. As necessidades de vitaminas solúveis em gordura (UI/d) estão na Tabela 1. Essas equações podem ser incorporadas a modelos preditivos. Recomendamos os requisitos ajustados em vez daqueles publicados pelo NASEM. Recomendamos aumentar as concentrações de vitamina A e D em 10% para levar em conta a oxidação normal das rações durante a fabricação e o armazenamento das rações. A Tabela 5 contém as inclusões recomendadas para as vitaminas lipossolúveis no substituto do leite e na ração iniciadora para fornecer a ingestão adequada para bezerros de 35 a 125 kg.
| NASEM | Ajustado | ||
| Vitamina | UI/dia | UI/dia (min) | |
| Vit A | 110 * PV | 110 * PV* 1.1 | |
| Vit D | 32 * PV | 32 * PV * 1,1 | |
| Vit E | 2 * PV | 2 * PV | |
| Vit E equivalente* | 4 * PV |
*Para bezerros alimentados com energia e proteína suficientes para atingir ≥700 g de GMD, recomendase um equivalente adicional de vitamina E. O equivalente de vitamina E pode ser fornecido por vitamina E ou precursores de vitamina E. PV = peso vivo corporal em quilogramas.
| NASEM, UI/kg DM | Ajustado, UI/kg DM | ||||||
| Vitamina | CMR | Início | Produtor | CMR | Início | Produtor | |
| Vit A | 11,000 | 3,700 | 3,700 | 11,000 | 4,500 | 4,500 | |
| Vit D | 3,200 | 1,100 | 1,100 | 3,500 | 1,300 | 1,300 | |
| Vit E | 200 | 67 | 67 | 200 | 80 | 80 | |
| Vit E equiv.* | 300 | 160 | 160 | ||||
*Para bezerros alimentados com energia e proteína suficientes para atingir ≥700 g de GMD, recomenda-se um equivalente adicional de vitamina E. O equivalente de vitamina E pode ser fornecido por vitamina E ou precursores de vitamina E.
Referências
Abuelo, A., J. Hernández, J. L. Benedito, and C. Castillo. 2019. Redox biology in transition periods of dairy cattle: Role in the health of periparturient and neonatal animals. Antioxidants (Basel). 13:20. https://doi.org/10.3390/antiox8010020.
Adams, C. 1982. Feedlot cattle need supplemental vitamin E. Feedstuffs. 54:24.
Blakely, L. P., M. B. Poindexter, R. L. Stuart, and C. D. Nelson. 2019. Supplementing pasteurized waste-milk with vitamins A, D, and E improves vitamin status of dairy calves. The Bovine Practitioner. 53:134–141. https://doi.org/10.21423/bovine-vol53no2p134-141.
Flores-Villalva, S., M. B. O’Brien, S. Reid, S. Lacey, S. V. Gordon, C. Nelson, and K. G. Meade. 2021. Low serum vitamin D concentrations in spring-born dairy calves are associated with elevated peripheral leukocytes. Sci. Rep. 11:18969. https://doi.org/10.1038/s41598-021-98343-8.
Jacobson, N. L., R. S. Allen, J. T. Blake, and P. G. Homeyer. 1954. The effect of method of administration on the absorption and storage of vitamin A by dairy calves: Two figures. J. Nutr. 54:143–153. https://doi.org/10.1093/jn/54.1.143.
Kume, S., and T. Toharmat. 2001. Effect of colostral β-carotene and vitamin A on vitamin and health status of newborn calves. Livestock Prod. Sci. 68:61-65. https://doi.org/10.1016/S0301-6226(00)00214-1.
Lashkari, S., S. K. Jensen, and M. Vestergaard. 2022. Response to different sources of vitamin E orally injected and to various doses of vitamin E in calf starter on the plasma vitamin E level in calves around weaning. Animal. 16:100492. https://doi.org/10.1016/j.animal.2022.100492.
Majlesi, A., S. P. Yasini, S. Azimpour, and P. Mottaghian. 2021. Evaluation of oxidative and antioxidant status in dairy calves before and after weaning. Bulg. J. Vet. Med. 24:184-190. https://doi.org/10.15547/bjvm.2270.
McDowell, L. R., S. N. Williams, N. Hidiroglou, C. A. Njeru, G. M. Hill, L. Ochoa, and N. S. Wilkinson. 1996. Vitamin E supplementation for the ruminant. Anim. Feed Sci. Technol. 60:273-296. https://doi.org/10.1016/0377-8401(96)00982-0.
Mohri, M. H., A. Seifi, and J. Khodadadi. 2005. Effects of preweaning parenteral supplementation of vitamin E and selenium on hematology, serum proteins, and weight gain in dairy calves. Comp. Clin. Pathol. 14: 149–154. https://doi.org/10.1007/s00580-005-0581-3.
National Academies of Sciences, Engineering, and Medicine. 2016. Nutrient Requirements of Beef Cattle: Eighth Revised Edition. Washington, DC: The National Academies Press. https://doi.org/10.17226/19014.
Nelson, C. D., J. D. Lippolis, T. A. Reinhardt, R. E. Sacco, J. L. Powell, M. E. Drewnoski, M. O’Neil, D. C. Beitz, and W. P. Weiss. 2016. Vitamin D status of dairy cattle: Outcomes of current practices in the dairy industry. J. Dairy Sci. 99:10150-10160. https://doi.org/10.3168/jds.2016-11727.
Nonnecke, B. J., M. R. Foote, B. L. Miller, D. C. Beitz, and R. L. Horst. 2010. Short communication: Fat-soluble vitamin and mineral status of milk. replacer-fed dairy calves: Effect of growth rate during the preruminant period. J. Dairy Sci. 93:2684–2690. https://doi.org/10.3168/jds.2009-2892.
Otomaru, K. S. Saito, K. Endo, M. Kohiruimaki, S. Fukuyama, and H. Ohtsuka. 2013. Effect of supplemental vitamin E on antibody titer in Japanese black calves vaccinated against bovine herpesvirus-1. J. Vet. Med. Sci. 75:1671–1673. https://doi.org/10.1292/jvms.13-0215.
Otomaru, K., S. Saito, K. Endo, M. Kohiruimaki, and H. Ohtsuka. 2015. Effect of supplemental vitamin E on the peripheral blood leukocyte population in Japanese Black calves. J. Vet. Med. Sci. 77:985–988. https://doi.org/10.1292/jvms.15-0060.
Pekmezci, D., and D. Cakiroglu. 2009. Investigation of immunomodulatory effects of levamisole and vitamin E on immunity and some blood parameters in newborn Jersey calves. Vet. Res. Commun. 33:711–721. https://doi.org/10.1007/s11259-009-9220-9.
Quigley III, J. D., and J. K. Bernard. 1995. Effects of addition of vitamin E to colostrum on serum α‐tocopherol and immunoglobulin concentrations in neonatal calves. Food and Ag. Immunol. 7:295-298. https://doi.org/10.1080/09540109509354887.
Rajaraman, V., B. J. Nonnecke, S. T. Franklin, D. C. Hammel, and R. L. Horst. 1998. Effects of vitamin A and E on nitric oxide production by blood mononuclear leukocytes from neonatal calves fed milk replacer. J. Dairy Sci. 81:3278–3285. https://doi.org/10.3168/jds.S0022-0302(98)75892-8.
Reddy, P. G., J. L. Morrill, and R. A. Frey. 1987a. Vitamin E requirements of dairy calves. J. Dairy Sci. 70:123-129. https://doi.org/10.3168/jds.S0022-0302(87)79987-1.
Reddy, P. G., J. L. Morrill, H. C. Minocha, and J. S. Stevenson. 1987b. Vitamin E is immunostimulatory in calves. J. Dairy Sci. 70:993-999. https://doi.org/10.3168/jds.S0022-0302(87)80104-2.
Schmidt, N., T. Luhmann, L. Hüther, U. Meyer, S. A. Barth, L. Geue, C. Menge, J. Frahm, and S. Dänicke. 2018. Effect of vitamin E supplementation in milk replacer and Shiga toxoid vaccination on serum α-tocopherol, performance, haematology and blood chemistry in male Holstein calves. Anim. Physiol. Anim. Nutr. 102:1167-1180. https://doi.org/10.1111/jpn.12926.
Waldner, C. L. and F. D. Uehlinger. 2016. Factors associated with serum vitamin A and vitamin E concentrations in beef calves from Alberta and Saskatchewan and the relationship between vitamin concentrations and calf health outcomes. Can. J. Anim. Sci. 97:65-82. https://doi.org/10.1139/cjas-2016-0055.
Wang, L. H., C. R. Zhang, Q. Y. Zhang, H. J. Xu, G. Z. Feng, G. N. Zhang, and Y. G. Zhang. 2022. Effects of feeding different doses of 25-hydroxyvitamin D3 on the growth performance, blood minerals, antioxidant status and immunoglobulin of preweaning calves. Anim. Feed Sci. Tech. 285:115220. https://doi.org/10.1016/j.anifeedsci.2022.115220.
Xu, H. J., L. H. Wang, Q. Y. Zhang, X. Jiang, C. R. Zhang, and Y. G. Zhang. 2021. Effects of 25-hydroxyvitamin D3 on growth performance, fecal scores, vitamin D3 metabolites, antioxidant status, and inflammatory and stress-related parameters in weaning calves. Anim. Feed Sci. Tech. 281:114946. https://doi.org/10.1016/j.anifeedsci.2021.114946.