Haga clic aquí para ver la versión en PDF
Introduction
La eficiencia aparente de absorción (EAA) se ha utilizado durante muchos años como una forma práctica de describir el éxito de la transferencia de IgG del calostro en el ternero recién nacido. El cálculo es sencillo: se estima la cantidad de IgG aparentemente presente en el ternero después de la alimentación, se divide por la cantidad de IgG ingerida y se expresa como un porcentaje. Este valor es útil porque nos permite comparar terneros, comparar programas de alimentación y evaluar el manejo. Sin embargo, la palabra aparente es importante.
Comencemos con un poco de contexto. Utilizamos la EAA para predecir la concentración sérica de IgG en un ternero en un momento determinado después del nacimiento:
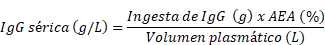
La ingesta de IgG es la concentración de IgG en el calostro × la cantidad de calostro consumida, y el volumen plasmático generalmente se calcula como el peso corporal (kg) × un factor para estimar el volumen plasmático, a menudo 9%.
Podemos reorganizar la ecuación para calcular la EAA:
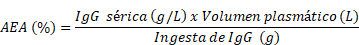
La EAA es una estimación de cuán eficiente es un ternero para absorber IgG del calostro. Algunos terneros, por supuesto, absorberán más IgG por unidad de IgG ingerida, y otros menos. Por lo tanto, es una medida importante del manejo del calostro en la granja. Factores como el estrés por calor preparto (Tao et al., 2012; Dado-Senn et al., 2020), la pasteurización del calostro (Elizondo-Salazar y Heinrichs, 2009; Robbers et al., 2021), y la distocia (Waldner et al., 2009; Murray et al., 2015), entre otros, han sido reportados como influyentes sobre la EAA.
Sin embargo, la EAA no es una medición directa de cuánta IgG cruzó la pared intestinal. Es una estimación basada en la concentración de IgG medida en suero o plasma, combinada con una estimación del volumen plasmático. Esto significa que el valor está influenciado no solo por la absorción intestinal, sino también por cómo la IgG se distribuye en los fluidos corporales después de ser absorbida. Por lo tanto, la EAA no es simplemente una medida de la absorción intestinal. También está influenciada por cómo la IgG se distribuye dentro del ternero después de ser absorbida. Esta distinción puede ayudar a explicar por qué la EAA nunca es del 100%, por qué varía tanto entre terneros y por qué parte de esa variación puede reflejar fisiología más allá de la absorción intestinal.
El concepto básico
Cuando un ternero consume calostro, la inmunoglobulina G (IgG) pasa del tracto intestinal al cuerpo mediante el proceso de pinocitosis. Pero una vez absorbida, la IgG no permanece únicamente en el torrente sanguíneo. En cambio, se distribuye entre al menos dos compartimentos de fluidos principales:
- el espacio vascular, es decir, el plasma dentro de los vasos sanguíneos
- el espacio extravascular, que incluye los fluidos intersticiales fuera de los vasos sanguíneos
Si medimos la IgG sérica en un momento determinado, estamos midiendo únicamente la concentración de IgG en el compartimento vascular en ese instante. No estamos midiendo la cantidad total de IgG absorbida en el cuerpo, sino cuánto IgG está presente en el espacio vascular en un momento específico.

Esto es importante porque la concentración sérica depende de:
- cuánto IgG ha sido absorbida, y
- en qué volumen de fluido se ha distribuido esa IgG
Por lo tanto, dos terneros pueden absorber cantidades similares de IgG, pero si la IgG se distribuye de manera diferente entre los espacios vascular y extravascular, la concentración sérica medida puede ser distinta.
“Espacio extravascular”
Fisiológicamente, los fluidos corporales se describen típicamente como compartimentos intracelulares y extracelulares. El fluido extracelular incluye tanto el plasma (dentro de los vasos sanguíneos) como el fluido intersticial (fuera de los vasos sanguíneos). El compartimento intracelular representa el fluido dentro de las células del cuerpo. Estos compartimentos se estiman utilizando marcadores específicos.
Las estimaciones del agua corporal total en terneros varían aproximadamente entre 72% y 88% del peso corporal (Thornton y English, 1975), basadas en investigaciones publicadas entre 1920 y 1975. La mayor parte del agua en los terneros se encuentra en el espacio extracelular: se ha reportado que el 80% o más del agua corporal total es extracelular (Wagstaff et al., 1992). Sin embargo, solo una pequeña parte de este fluido se encuentra dentro del espacio vascular donde se mide la IgG sérica.
Cuando consideramos la absorción de IgG, normalmente medimos el volumen plasmático (VP), que forma parte del compartimento extracelular. El volumen plasmático en terneros se mide generalmente utilizando marcadores como el azul de Evans (Thornton y English, 1978; Wagstaff et al., 1992; Quigley et al., 1998; Cabral et al., 2015) o radioisótopos como la albúmina sérica marcada con ¹³¹I (Möllerberg et al., 1975; Wagstaff et al., 1992).
Para entender la absorción de IgG, es útil considerar dos compartimentos funcionales: el espacio vascular, donde medimos la IgG, y el espacio extravascular, donde la IgG también puede distribuirse después de la absorción.
Consideremos un ejemplo de un ternero de 40 kg a 1 día de edad para calcular los compartimentos de agua corporal y analizar la naturaleza dinámica de las mediciones de IgG sérica:
- Peso corporal (PC) = 40 kg
- Agua corporal total (ACT) = 40 × 0.75 = 30 kg
- Fluido extracelular = 30 × 0.80 = 24 kg
- Fluido intracelular = 30 − 24 = 6 kg
- Volumen plasmático = 40 × 0.09 = 3.6 kg
- Fluido intersticial = 24 − 3.6 = 20.4 kg
En este ejemplo, el ternero tiene aproximadamente 24 kg de fluido extracelular, pero solo 3.6 kg están en el espacio vascular donde se mide la IgG sérica. La relación entre fluido intersticial y plasma es aproximadamente 5.7:1; es decir, el compartimento intersticial es casi seis veces mayor que el compartimento plasmático.
Volumen de distribución
En farmacología, la distribución de una sustancia entre los compartimentos vascular y extravascular se describe mediante el concepto de volumen de distribución (Vd). Este valor refleja el grado en que un compuesto se mueve fuera del torrente sanguíneo hacia los tejidos y fluidos circundantes. Es importante destacar que el Vd no necesariamente corresponde a un volumen físico o anatómico. Más bien, representa el volumen aparente en el cual una sustancia se ha distribuido en el momento de la medición.
Este concepto puede ser útil al considerar la IgG en el ternero recién nacido. Aunque el espacio total extravascular es varias veces mayor que el volumen plasmático, la IgG no parece distribuirse de manera uniforme ni instantánea en todo este espacio. En cambio, la distribución observada entre los compartimentos vascular y extravascular es mucho menor, aproximadamente 1.3:1. Esto es mucho menor que la relación anatómica, lo que indica que la IgG ha equilibrado solo una parte del espacio extravascular al momento de la medición.
La IgG se distribuye en fluidos extravascular, incluyendo el espacio intersticial, lo cual ha sido demostrado en múltiples especies mediante mediciones en linfa y fluidos tisulares. Por lo tanto, la concentración sérica de IgG refleja el equilibrio entre absorción y distribución, no solo la absorción.
Por qué la EAA nunca será 100%
En condiciones de campo, y probablemente incluso en condiciones experimentales ideales, no se debe esperar que la EAA alcance el 100%. Existen varias razones para esto.
Primero, no toda la IgG ingerida es absorbida. La absorción intestinal es inherentemente incompleta.
Segundo, la EAA se basa en la concentración de IgG en suero o plasma, no en la cantidad total de IgG en el cuerpo. Si parte de la IgG se ha distribuido en el espacio extravascular al momento del muestreo, la medición en plasma subestimará la cantidad total absorbida.
Tercero, la distribución de la IgG es dinámica. A medida que la IgG se mueve entre los compartimentos vascular y extravascular, la concentración sérica cambia con el tiempo, incluso si la cantidad total de IgG en el cuerpo no cambia.
Un sistema dinámico, no estático
Uno de los errores más comunes es pensar en la absorción de IgG como un evento simple. En realidad, es un proceso dinámico.
La concentración sérica de IgG en cualquier momento es una “instantánea” de un sistema fisiológico en movimiento.
Resumen
Nuestras estimaciones de EAA representan una medición en un momento específico dentro de un sistema dinámico. La EAA refleja no solo la absorción de IgG, sino también su distribución dentro del cuerpo del ternero.
Referencias
Cabral, R. G., C. E. Chapman, E. J. Kent, and P. S. Erickson. 2015. Estimating plasma volume in neonatal Holstein calves fed one or two feedings of a lacteal-based colostrum replacer using Evans blue dye and hematocrit values at various time points. Can. J. Anim. Sci. 95:293-298 doi:10.4141/CJAS-2014-176 293.
Dado-Senn, B., L. Vega Acosta, M. Torres Rivera, S. L. Field, M. G. Marrero, B. D. Davidson, S. Tao, T. F. Fabris, G. Ortiz-Colón, G. E. Dahl, and J. Laporta. Pre- and postnatal heat stress abatement affects dairy calf thermoregulation and performance. J. Dairy Sci. 103:4822-4837. https://doi.org/10.3168/jds.2019-17926.
Elizondo-Salazar, J. A., and A. J. Heinrichs. 2009. Feeding heat-treated colostrum or unheated colostrum with two different bacterial concentrations to neonatal dairy calves. J. Dairy Sci. 92 :4565–4571 doi:10.3168/jds.2009-2188.
Möllerberg, L., L. Ekman and S. Jacobsson. 1975. Plasma and blood volume in the calf from birth till 90 days of age. Acta Vet. Scand. 16:178-185.
Murray, C. F., D. M. Veira, A. L. Nadalin, D. M. Haines, M. L. Jackson, D. L. Pearl, and K. E Leslie. 2015. The effect of dystocia on physiological and behavioral characteristics related to vitality and passive transfer of immunoglobulins in newborn Holstein calves. Can. J. Vet. Res. 79:109–119.
Quigley, J. D. III, J. J. Drewry, and K. R. Martin. 1998. Estimation of plasma volume in Holstein and Jersey calves. J. Dairy Sci. 81:1308-1312.
Robbers, L., R. Jorritsma, M. Nielen, and A. Koets. 2021. A scoping review of on-farm colostrum management practices for optimal transfer of immunity in dairy calves. Front. Vet. Sci., 18 July 2021. 8-2021. https://doi.org/10.3389/fvets.2021.668639.
Tao, S., A. P. A. Monteiro, I. M. Thompson, M. J. Hayen, and G. E. Dahl. 2012. Effect of late-gestation maternal heat stress on growth and immune function of dairy calves. J. Dairy Sci. 95:7128–7136. http://dx.doi.org/ 10.3168/jds.2012-5697.
Thornton, J. R., and P. B. English. 1978. Body water of calves: Change in distribution with diarrhoea. Br. Vet. J. 134:445-453.
Wagstaff, A. J., I. Maclean, A. R. Michell, and P. H. Holmes. 1992. Plasma and extracellular volume in calves: comparison between isotopic and ‘cold’ techniques. Res. Vet. Sci., 53:271-273.
Waldner, C. L., and L. B. Rosengren . 2009. Factors associated with serum immunoglobulin levels in beef calves from Alberta and Saskatchewan and association between passive transfer and health outcomes. Can Vet J. 50:275–281.